Сабақ жоспарлары / Физика
Атомдардың сәуле шығару және сәуле жұту спектрлері. Бор пастулаттары. - Физика, 9 сынып, 47 - сабақ
Сабақтың тақырыбы: Атомдардың сәуле шығару және сәуле жұту спектрлері. Бор пастулаттары.

Сабақтың мақсаты:
Сабақтың әдіс-тәсілдері: Әңгіме, лекция, дискуссия, кітаппен жұмыс.
Сабақтың көрнекіліктері: плакаттар, суреттер,
Сабақтың барысы:
І. ДК. Ұйымдастыру кезеңі:
1. Сәлемдесу;
2. Оқушыларды түгендеу;
3. Сынып болмесінің тазалығын тексеру;
4. Оқушылардың сабаққа дайындығын тексеру (жұмыс орны, отырыстары, сыртқы түрлері);
5. Оқушылардың назарын сабаққа аудару.
ІІ. ДК. Үй тапсырмасын тексеру, қайталау.
А) теориялық білімдерін тексеру.
Ә) практикалық тапсырмаларын тексеру.
Б) есептерін тексеру.
ІІІ.ДК Білімді жан-жақты тексеру./ ІV. ДК. Жаңа материалды қабылдауға әзірлік, мақсат қою.
Бүгінгі негізгі мақсатымыз оқулық бойынша атомдардың сәуле шығару және сәуле жұту спектрлерімен Бор пастулаттарымен танысамыз.
Табиғаттағы процестер туралы кванттық түсініктерді одан әрі дамыта отырып, 1913 ж. Данияның ұлы физигі Нильс Бор физиктерді ойландырған өте қиын жағдайдан шығарудың жолын тапты.
Бордың еңбегіне сүйенген Эйнштейн, оны "ақыл-ой саласындағы жоғары музыкалық дарын" деп бағалады. Бір-біріне дара жатқан тәжірибе деректеріне сүйене отырып, Бор данышпандық түйсіктің жәрдемімен істің мәнін дұрыс аңғарды.
Бор постулаттары. Бор жүйелі атом теориясын берген жоқ. Ол жаңа теорияның негізгі қағидаларын постулаттар түрінде тұжырымдап берді. Сонымен бірге классикалық физиканың заңдарынан да ол қол үзген жоқ. Дәлірек айтқанда, жаңа постулаттар классикалық физикада рұқсат етілетін қозғалысқа кейбір шектеулер ғана қойды.
Осыған қарамастан, Бор теориясының табысы айтарлықтай болып, Бордың теорияны дамытудың дұрыс жолын тапқандығы барлық ғылымдарға айқын болды. Осы жол кейіннен микробөлшектер қозғалысының тыңғылықты теориясы — кванттық механиканың шығуына себепші болды.
Бордың бірінші постулатында былай делінген: атомдық жүйе тек ерекше стационар немесе кванттық күйлерде ғана болады, олардың әрқайсысына белгілі бір энергия Еn сәйкес келеді. Стационар күйде атом сәуле шығармайды.
Бұл постулат қозғалыстағы электрондардың энергиясы кез келген мән қабылдайды дейтін классикалық механикаға тікелей қайшы келеді. Ол Максвеллдің электродинамикасына да қайшы келеді, себебі электрондар электромагниттік толқынды шығармай-ақ, үдемелі қозғала алатындығын айтады.
Бордың екінші постулатына сәйкес, атом үлкен энергиялы Ек стационар күйден аз энергиялы Еn стационар күйге өткенде жарық шығарылады. Шығарылған фотонның энергиясы атомның стационар екі күйдегі энергияларының айырымына тең: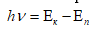 (2) Бұдан сәуле шығару жиілігін былай өрнектеуге болады:
(2) Бұдан сәуле шығару жиілігін былай өрнектеуге болады:
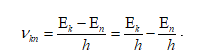 Жарықтың жұтылу кезінде атом энергиясы аз стационар күйден энергиясы көп стационар күйге өтеді.
Жарықтың жұтылу кезінде атом энергиясы аз стационар күйден энергиясы көп стационар күйге өтеді.
Екінші постулат та Максвеллдің электродинамикасына қайшы, өйткені сол постулатқа сәйкес шығарылған жарықтың жиілігі электрондардың қозғалыс ерекшеліктерін сипаттамайды, тек атом энергиясының өзгерісін ғана көрсетеді. Бор өзінің постулаттарын қарапайым атомның сутегі атомының теориясын жасау үшін қолданды. Негізгі мақсат сутегі шығаратын электромагниттік толқындардың жиіліктерін табу болды. Бұл жиіліктерді, егер атом энергиясының стационар мәндерін анықтау ережесі бар болса, екінші постулат негізінде табуға болды. Бордың бұл ережені (кванттау ережесі деп аталатын) тағы да постулаттауына тура келді.
Бор жасаған сутегі атомының моделі. Жарықтың жұтылуы
Ньютон механикасының заңдарын және мүмкін болатын стационар күйлерді иеленетін кванттау ережесін пайдаланып, Бор электрон орбиталарының қажетті радиустары мен стационар күйлер энергиясын есептеп шығара алды. Орбитаның ең кіші радиусы атомның өлшемдерін анықтайды. 1, а, б-суреттерде стационар күйлер энергиясы (электрон-вольтпен есептелген) вертикаль осьтерге өлшеп салынған. Бордың екінші постулаты стационар күйлер энергиясының белгілі мәндері бойынша сутегі атомы шығаратын сәуленің жиілігін есептеп шығаруға мүмкіндік берді. Бор теориясы осы жиіліктердің мәндеріне арналған экспериментпен сандық тұрғыда үйлесуге келтіреді. Сутегі атомы шығаратын сәулелердің барлық жиіліктері сериялар қатарын құрады, олардың әрқайсысы атом барлық жоғары энергетикалық күйлерден (энергиясы көп күйлер) кейбір энергетикалық күйге (екінші энергетикалық деңгейге) өткенде Бальмер сериясы түзіледі. 1, а-суретте бұл ауысулар бағыттауыштармен кескінделген. Сутегі спектрінің көрінетін бөлігіндегі қызыл, жасыл және екі көк сызық (3-түсті жапсырма, V сурет) мынадай ауысуларға сәйкес келеді:
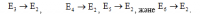
Берілген серия Швейцар мұғалімі И. Бальмер есімімен аталған, ол тіпті 1885 жылы эксперимент негізінде сутегі спектрінің көрінетін бөлігінің жиіліктерін анықтау үшін қарапайым формула тағайындады.
Жарықтың жұтылуы. Жарықтың жұтылуы - сәуле шығаруға кері процесс. Атом, жарықты жұта отырып, төменгі энергетикалық күйлерден жоғарғыға өтеді. Бұл жағдайда жұтылатън жарықтың жиілігі атом жоғарғы энергетикалық күйлерден төмендегілеріне өткенде шығаратын жарықтың жиілігіндей болады. 1, б-суретте атомның бір күйден екінші күйге жарық жұта отырып өтуі бағыттауыштармен кескінделген.
Екі постулат пен кванттау ережесі негізінде Бор сутегі атомының радиусын және атомның стационар күйлерінің энергиясын анықтады. Бұл атомның шығаратын және жұтатын электромагниттік толқындарының жиіліктерін есептеуге мүмкіндік берді
БОР ТЕОРИЯСЫНЫҢ ҚИЫНШШЫЛЫҚТАРЫ. КВАНТТЫҚ МЕХАНИКА
Бор теориясын сутегі атомына қолдану өте табысты болып, ол үшін спектрдің сандық теориясын жасау мүмкін болды. Бірақ Бордың постулаттарына сүйеніп, сутегінен кейінгі гелий атомының сандық теориясын жасау мақсатынан ештеңе шықпады. Гелий атомы және одан да күрделі атомдар үшін Бор теориясына сүйеніп, тек сапалық (бірақ аса маңызды) тұжырымдар жасауға ғана мүмкіңдік болды.
Мұнда таңданарлық ештеңе жоқ. Бор теориясы сыңаржақты, оның ішкі қайшылықтары бар, бір жағынан өзіміз көргендей, сутегі атомының теориясын жасағанда кәдімгі Ньютон заңы пайдаланылса, екінші жағынан Ньютон механикасымен, Максвелл элекгродинамикасымен ешқандай байланысы жоқ кванттық постулаттар енгізіледі. Физикаға квантық түсініктерді енгізу механика мен электродинамиканы түбегейлі түрде қайта құруды талап етгі. Бұл қайта құру біздің ғасырдың екінші ширегінің басында іске асты. Кванттық механика мен кванттық электродинамика сияқты физикалық теориялар жасалды. Бордың постулаттары әбден дұрыс болып шықты. Бірақ олар постулаттар емес, осы теориялардың негізгі принциптерінің салдары болып қана қалды. Ал Бордың кванттау ережесі кез келген жерде қолданыла бермейтін болып шықты. Бор атомында электрон қозғалатын белгілі орбиталар туралы ұғым тек шартты түсінік болып табылады. Шындығында, атомдағы электрон қозғалысының планеталардың өз орбиталары бойымен қозғаласына ұқсастығы жоққа тән. Егер ең төменгі энергетикалық күйдегі сутегі атомын ұзақ ұстап, суретке түсіріп алу мүмкін болса, онда біз тығыздығы айнымалы бұлт көрген болар едік. Көбінесе элекрон ядродан белгілі бір қашықтықта жүреді. Бұл қашықтықты дөрекі түрде орбитаның радиусына ұқсатуға болады. Атомның фотосуреті Күн жүйесінің әдеттегі суретіне мүлде ұқсамайды, шамды айнала ретсіз ерсілі-қарсылы ұшқан көбелектерді суретке түсірген кезде шыққан жайылған дақты еске түсіреді.
Қазіргі кезде кванттық механиканың көмегімен атомдардың электрондық қабықшаларының қасиеттері мен құрылысына қатысты барлық сұрақтарға жауап беруге болады. Бірақ сандық теория аса күрделі болғандықтан, біз оған соқпай өтеміз. Атомдардың электрондық қабықшаларының сапалық сипаттамасымен сендер химия курсында танысасыңдар.
VІ. ДК. Оқытылып отырған оқу материалын қабылдаудағы оқушы түсінігін тексеру.
§55 дайындық сұрақтарын талдау.
VІІ. ДК. Оқытылып отырған оқу материалын бекіту немесе дағдыландыру жұмыстарын жүргізу.
К., Т., №16.24-16.27
VIІI.ДК. Бағалау. Үй тапсырмасын беру: §55 дайындық сұрақтары. 43-жаттығу
- Білімділік мақсаты: Оқушы білімін, іскерлігін, дағды деңгейін бақылау, бағалау. Атомдардың сәуле шығару және сәуле жұту спектрлері мен Бор пастулаттары туралы негізгі ұғымдармен таныстырып солар жайлы түсінік қалыптастыру.
- Дамытушылық мақсаты: Оқушылардың білім деңгейін және білім мазмұнының тұрақтылығы мен оны игерудегі іскерлік пен дағдыны бақылау.
- Тәрбиелік мақсаты: Адамгершілікке, ұқыптылыққа, алғырлыққа, отансүйгіштікке, табиғатты аялауға, сыйластық пен әдептілікке баулу.
Сабақтың әдіс-тәсілдері: Әңгіме, лекция, дискуссия, кітаппен жұмыс.
Сабақтың көрнекіліктері: плакаттар, суреттер,
Сабақтың барысы:
І. ДК. Ұйымдастыру кезеңі:
1. Сәлемдесу;
2. Оқушыларды түгендеу;
3. Сынып болмесінің тазалығын тексеру;
4. Оқушылардың сабаққа дайындығын тексеру (жұмыс орны, отырыстары, сыртқы түрлері);
5. Оқушылардың назарын сабаққа аудару.
ІІ. ДК. Үй тапсырмасын тексеру, қайталау.
А) теориялық білімдерін тексеру.
Ә) практикалық тапсырмаларын тексеру.
Б) есептерін тексеру.
ІІІ.ДК Білімді жан-жақты тексеру./ ІV. ДК. Жаңа материалды қабылдауға әзірлік, мақсат қою.
Бүгінгі негізгі мақсатымыз оқулық бойынша атомдардың сәуле шығару және сәуле жұту спектрлерімен Бор пастулаттарымен танысамыз.
- Қандай элементтер радиоактивті элементтер дейді?
- Радиактивті сәулелену дегеніміз не?
- Атомның планетааралық моделі қандай тәжірибеге негізделген?
- Атом ядросының құрамы қандай?
Табиғаттағы процестер туралы кванттық түсініктерді одан әрі дамыта отырып, 1913 ж. Данияның ұлы физигі Нильс Бор физиктерді ойландырған өте қиын жағдайдан шығарудың жолын тапты.
Бордың еңбегіне сүйенген Эйнштейн, оны "ақыл-ой саласындағы жоғары музыкалық дарын" деп бағалады. Бір-біріне дара жатқан тәжірибе деректеріне сүйене отырып, Бор данышпандық түйсіктің жәрдемімен істің мәнін дұрыс аңғарды.
Бор постулаттары. Бор жүйелі атом теориясын берген жоқ. Ол жаңа теорияның негізгі қағидаларын постулаттар түрінде тұжырымдап берді. Сонымен бірге классикалық физиканың заңдарынан да ол қол үзген жоқ. Дәлірек айтқанда, жаңа постулаттар классикалық физикада рұқсат етілетін қозғалысқа кейбір шектеулер ғана қойды.
Осыған қарамастан, Бор теориясының табысы айтарлықтай болып, Бордың теорияны дамытудың дұрыс жолын тапқандығы барлық ғылымдарға айқын болды. Осы жол кейіннен микробөлшектер қозғалысының тыңғылықты теориясы — кванттық механиканың шығуына себепші болды.
Бордың бірінші постулатында былай делінген: атомдық жүйе тек ерекше стационар немесе кванттық күйлерде ғана болады, олардың әрқайсысына белгілі бір энергия Еn сәйкес келеді. Стационар күйде атом сәуле шығармайды.
Бұл постулат қозғалыстағы электрондардың энергиясы кез келген мән қабылдайды дейтін классикалық механикаға тікелей қайшы келеді. Ол Максвеллдің электродинамикасына да қайшы келеді, себебі электрондар электромагниттік толқынды шығармай-ақ, үдемелі қозғала алатындығын айтады.
Бордың екінші постулатына сәйкес, атом үлкен энергиялы Ек стационар күйден аз энергиялы Еn стационар күйге өткенде жарық шығарылады. Шығарылған фотонның энергиясы атомның стационар екі күйдегі энергияларының айырымына тең:
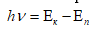 (2) Бұдан сәуле шығару жиілігін былай өрнектеуге болады:
(2) Бұдан сәуле шығару жиілігін былай өрнектеуге болады: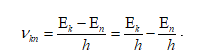 Жарықтың жұтылу кезінде атом энергиясы аз стационар күйден энергиясы көп стационар күйге өтеді.
Жарықтың жұтылу кезінде атом энергиясы аз стационар күйден энергиясы көп стационар күйге өтеді.Екінші постулат та Максвеллдің электродинамикасына қайшы, өйткені сол постулатқа сәйкес шығарылған жарықтың жиілігі электрондардың қозғалыс ерекшеліктерін сипаттамайды, тек атом энергиясының өзгерісін ғана көрсетеді. Бор өзінің постулаттарын қарапайым атомның сутегі атомының теориясын жасау үшін қолданды. Негізгі мақсат сутегі шығаратын электромагниттік толқындардың жиіліктерін табу болды. Бұл жиіліктерді, егер атом энергиясының стационар мәндерін анықтау ережесі бар болса, екінші постулат негізінде табуға болды. Бордың бұл ережені (кванттау ережесі деп аталатын) тағы да постулаттауына тура келді.
Бор жасаған сутегі атомының моделі. Жарықтың жұтылуы
Ньютон механикасының заңдарын және мүмкін болатын стационар күйлерді иеленетін кванттау ережесін пайдаланып, Бор электрон орбиталарының қажетті радиустары мен стационар күйлер энергиясын есептеп шығара алды. Орбитаның ең кіші радиусы атомның өлшемдерін анықтайды. 1, а, б-суреттерде стационар күйлер энергиясы (электрон-вольтпен есептелген) вертикаль осьтерге өлшеп салынған. Бордың екінші постулаты стационар күйлер энергиясының белгілі мәндері бойынша сутегі атомы шығаратын сәуленің жиілігін есептеп шығаруға мүмкіндік берді. Бор теориясы осы жиіліктердің мәндеріне арналған экспериментпен сандық тұрғыда үйлесуге келтіреді. Сутегі атомы шығаратын сәулелердің барлық жиіліктері сериялар қатарын құрады, олардың әрқайсысы атом барлық жоғары энергетикалық күйлерден (энергиясы көп күйлер) кейбір энергетикалық күйге (екінші энергетикалық деңгейге) өткенде Бальмер сериясы түзіледі. 1, а-суретте бұл ауысулар бағыттауыштармен кескінделген. Сутегі спектрінің көрінетін бөлігіндегі қызыл, жасыл және екі көк сызық (3-түсті жапсырма, V сурет) мынадай ауысуларға сәйкес келеді:
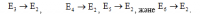
Берілген серия Швейцар мұғалімі И. Бальмер есімімен аталған, ол тіпті 1885 жылы эксперимент негізінде сутегі спектрінің көрінетін бөлігінің жиіліктерін анықтау үшін қарапайым формула тағайындады.
Жарықтың жұтылуы. Жарықтың жұтылуы - сәуле шығаруға кері процесс. Атом, жарықты жұта отырып, төменгі энергетикалық күйлерден жоғарғыға өтеді. Бұл жағдайда жұтылатън жарықтың жиілігі атом жоғарғы энергетикалық күйлерден төмендегілеріне өткенде шығаратын жарықтың жиілігіндей болады. 1, б-суретте атомның бір күйден екінші күйге жарық жұта отырып өтуі бағыттауыштармен кескінделген.
Екі постулат пен кванттау ережесі негізінде Бор сутегі атомының радиусын және атомның стационар күйлерінің энергиясын анықтады. Бұл атомның шығаратын және жұтатын электромагниттік толқындарының жиіліктерін есептеуге мүмкіндік берді
БОР ТЕОРИЯСЫНЫҢ ҚИЫНШШЫЛЫҚТАРЫ. КВАНТТЫҚ МЕХАНИКА
Бор теориясын сутегі атомына қолдану өте табысты болып, ол үшін спектрдің сандық теориясын жасау мүмкін болды. Бірақ Бордың постулаттарына сүйеніп, сутегінен кейінгі гелий атомының сандық теориясын жасау мақсатынан ештеңе шықпады. Гелий атомы және одан да күрделі атомдар үшін Бор теориясына сүйеніп, тек сапалық (бірақ аса маңызды) тұжырымдар жасауға ғана мүмкіңдік болды.
Мұнда таңданарлық ештеңе жоқ. Бор теориясы сыңаржақты, оның ішкі қайшылықтары бар, бір жағынан өзіміз көргендей, сутегі атомының теориясын жасағанда кәдімгі Ньютон заңы пайдаланылса, екінші жағынан Ньютон механикасымен, Максвелл элекгродинамикасымен ешқандай байланысы жоқ кванттық постулаттар енгізіледі. Физикаға квантық түсініктерді енгізу механика мен электродинамиканы түбегейлі түрде қайта құруды талап етгі. Бұл қайта құру біздің ғасырдың екінші ширегінің басында іске асты. Кванттық механика мен кванттық электродинамика сияқты физикалық теориялар жасалды. Бордың постулаттары әбден дұрыс болып шықты. Бірақ олар постулаттар емес, осы теориялардың негізгі принциптерінің салдары болып қана қалды. Ал Бордың кванттау ережесі кез келген жерде қолданыла бермейтін болып шықты. Бор атомында электрон қозғалатын белгілі орбиталар туралы ұғым тек шартты түсінік болып табылады. Шындығында, атомдағы электрон қозғалысының планеталардың өз орбиталары бойымен қозғаласына ұқсастығы жоққа тән. Егер ең төменгі энергетикалық күйдегі сутегі атомын ұзақ ұстап, суретке түсіріп алу мүмкін болса, онда біз тығыздығы айнымалы бұлт көрген болар едік. Көбінесе элекрон ядродан белгілі бір қашықтықта жүреді. Бұл қашықтықты дөрекі түрде орбитаның радиусына ұқсатуға болады. Атомның фотосуреті Күн жүйесінің әдеттегі суретіне мүлде ұқсамайды, шамды айнала ретсіз ерсілі-қарсылы ұшқан көбелектерді суретке түсірген кезде шыққан жайылған дақты еске түсіреді.
Қазіргі кезде кванттық механиканың көмегімен атомдардың электрондық қабықшаларының қасиеттері мен құрылысына қатысты барлық сұрақтарға жауап беруге болады. Бірақ сандық теория аса күрделі болғандықтан, біз оған соқпай өтеміз. Атомдардың электрондық қабықшаларының сапалық сипаттамасымен сендер химия курсында танысасыңдар.
VІ. ДК. Оқытылып отырған оқу материалын қабылдаудағы оқушы түсінігін тексеру.
§55 дайындық сұрақтарын талдау.
VІІ. ДК. Оқытылып отырған оқу материалын бекіту немесе дағдыландыру жұмыстарын жүргізу.
К., Т., №16.24-16.27
VIІI.ДК. Бағалау. Үй тапсырмасын беру: §55 дайындық сұрақтары. 43-жаттығу
Пікір қалдыру (0)
Пікірлер:
Ұқсас жаңалықтар:
Басқа жаңалықтар:

Атомның күрделі құрылысын айғақтайтын құбылыстар. - Физика, 9 сынып, 46 - сабақ

Рентгендік сәуле шығару. Есеп шығару. - Физика, 9 сынып, 45 - сабақ

Жарық кванттары туралы Планк гипотезасы. Планк формуласы. - Физика, 9 сынып, 44 - сабақ

Жылулық сәулелену. Абсалют қара дене. - Физика, 9 сынып, 43 - сабақ


